
2025年9月的CSCO年会,一份重磅文件的发布让肺癌靶向治疗再掀热潮——《EGFR PACC突变晚期非小细胞肺癌诊疗专家共识(2025 版)》正式亮相。这是全球首个聚焦EGFR PACC突变的系统性临床诊疗指南,给原本就备受瞩目的EGFR突变赛道增添了新的焦点。
虽说EGFR突变早已是肺癌靶向药物开发的“明星赛道”:从2003年吉非替尼(第一代EGFR-TKI药物)获批至今,20余年时间内EGFR-TKI药物历经4代发展,让无数EGFR突变的非小细胞肺癌(NSCLC)患者生存期大幅延长。然而,EGFR突变亚型繁杂,已上市的EGFR-TKI药物虽对ex19del、L858R等经典突变有较好疗效,但仍有大量罕见突变患者由于缺乏有效靶向治疗药物,预后依旧不理想。
而PACC突变就是这类罕见突变中的“大家族”——它是一类罕见突变的总称,约占所有EGFR突变的12.5%,是仅次于经典突变的第二大亚型。由于PACC突变存在诊断困难、亚型繁杂、异质性强、不同亚型对不同EGFR-TKI敏感性差异大等问题,目前,全球范围内均无针对此类突变的一线治疗EGFR-TKI药物上市。然而,PACC突变不仅患者数量众多、未满足的临床需求巨大,而且其作为2021年刚被明确界定出来的新的突变亚型,在指导临床诊疗、药物开发方面意义重大,正在成为药企竞速的新战场。要读懂它的价值,我们首先得从EGFR突变的“分型革命”讲起。
从位置分型到结构分型:一场迟到的分型革命
在很长一段时间内,EGFR突变的分型是按照“外显子位置+突变频率+药物敏感性”进行分类的,虽然直观易用,但对临床精准用药的指导价值有限。例如虽然很多突变位于同一外显子,但它们导致的激酶结构不同,因此对同一类EGFR-TKI的敏感性存在很大差异。此外,传统分类中通常将所有罕见突变归于一类,缺乏细分的治疗方案,给临床诊疗造成了很大困扰。
2021年,MD Anderson癌症中心在EGFR突变传统分型的基础上,提出了一个新的、基于结构的分型方法。根据突变的分子特征、药物敏感性及结构-功能相关性将EGFR突变重新分成4大类。这种全新的分型方式为靶向治疗策略的优化提供了理论基础。其中ex20ins突变和PACC突变作为两种罕见突变类型,凭借共约20%的占比和未被满足的临床需求,迅速从"小众赛道"跃升为"必争之地"。
MD Anderson癌症中心EGFR突变亚型分类1
|
突变亚型 |
Classical-like |
T790M-like |
Exon20ins |
PACC |
|
|
|
|
|
|
|
突变特征 |
距离药物结合口袋较远,对药物结合影响轻微甚至无影响 |
至少有一个突变在疏水核心区,对药物结合产生一定影响 |
通过影响αC螺旋的C端环状结构,对药物结合产生显著影响 |
突变位点靠近药物结合口袋,通过 P环和/或αC螺旋的中度偏移,对药物结合产生显著影响 |
|
代表突变 |
ex19del、L858R、L861Q等 |
Classical/T790M、Classical/T790M/C797S等 |
S768dupSVD、A767dupASV等上百种突变亚型 |
G719X等原始突变;C797S、G724S等获得性突变,数十种突变亚型 |
|
突变占比 |
67.1% |
~10% |
4-10% |
12.5% |
|
已上市的一线EGFR-TKI |
1-3代EGFR-TKI |
个别亚型可选3代EGFR-TKI |
尚无 |
尚无 |
EGFR PACC突变:未满足临床需求巨大,机遇与挑战共存
PACC突变的全称是“P环与αC螺旋压缩突变”,是一类罕见突变的总称,其特点为相关突变会导致P环和/或αC螺旋压缩,使疏水区域空间收到压缩、药物结合口袋空间变小,进而影响其与药物分子的稳定结合,限制了传统EGFR-TKI疗效。尽管临床患者人数众多,但PACC的突变亚型亦繁多,横跨18-21外显子,目前已经鉴定出的单一亚型数量便有数十种。且该类突变经常发生复合突变,导致临床诊疗难度进一步加大。
常见的PACC突变位点
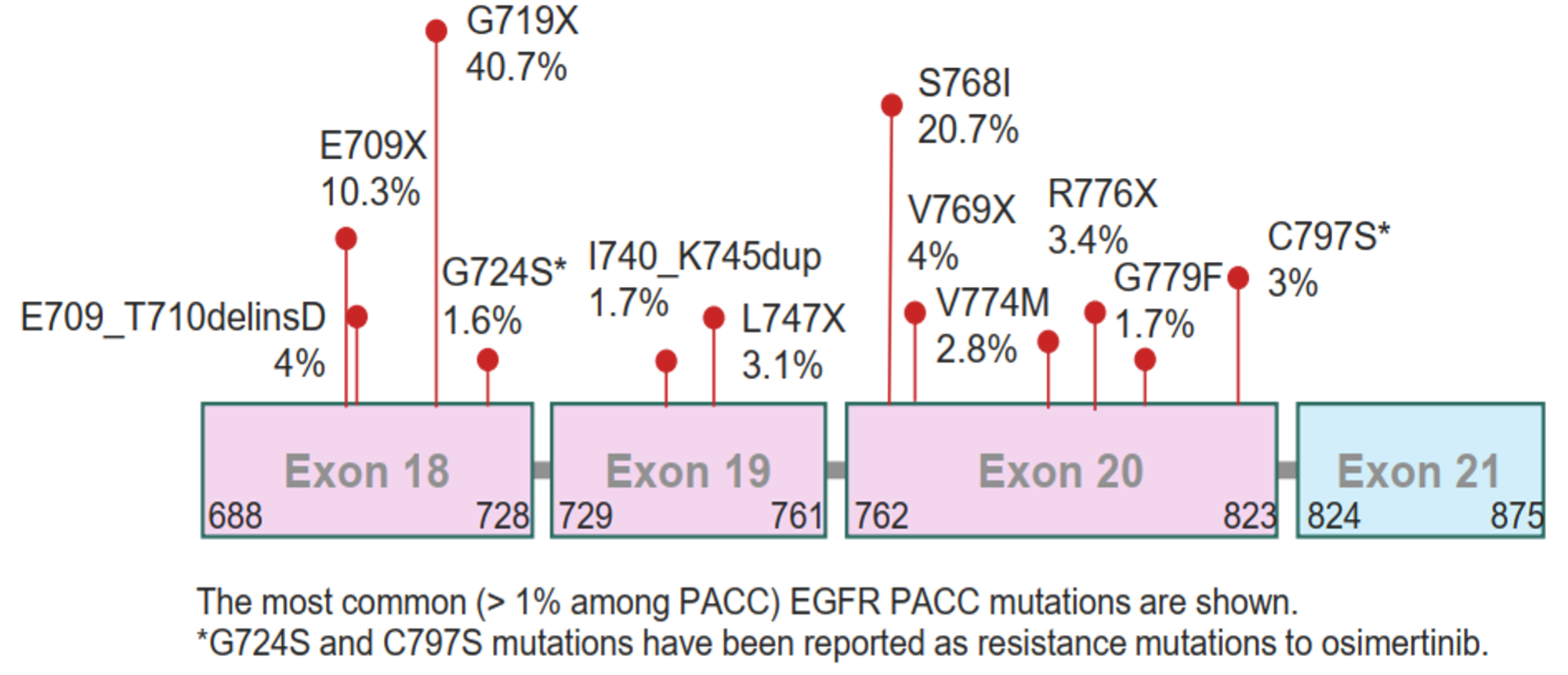
精确诊断是PACC突变患者临床诊疗需要迈过的第一道“坎”。目前临床上常用的突变检测方法仍为PCR,其仅能覆盖S768I、G719C等少数PACC突变位点,大量突变无法检出,导致漏检率极高。一旦出现漏检,临床上极有可能误认为患者为EGFR野生型患者,采用传统化疗进行治疗,导致患者生存期大大缩短。在《EGFR PACC 突变晚期非小细胞肺癌诊疗专家共识(2025 版)》中明确提到“建议晚期NSCLC在治疗前进行EGFR PACC突变检测,检测方法优先推荐NGS”。
在治疗端,由于PACC突变复杂、合并突变多、患者异质性强,不同的突变位点对1-3代EGFR-TKI的敏感性存在显著差异,这给临床的治疗决策也提出了很大的挑战。
过往研究表明,第二代EGFR-TKI(例如阿法替尼)在PACC突变患者人群中展现出更好的疗效,但其针对不同亚型的有效性存在明显差异且临床证据有限,已有证据的临床获益几乎都局限在G719X和S768I突变位点。此外,第二代EGFR-TKI的安全性问题不容忽视,其治疗相关任何级别不良反应的发生率约为93.8%~97%,≥3级不良反应发生率高达44%2,且部分严重不良事件(如肺炎)可能影响临床结局。安全性的问题一直是第二代EGFR-TKI在临床大规模应用的一大阻碍。
更安全、更广泛:新一代EGFR-TKI的破局之路
截至2025年12月,已有多家企业正在积极布局针对PACC突变的新一代EGFR-TKI药物,部分临床试验信息如下:
部分正在开展的针对EGFR PACC突变的EGFR-TKI药物临床试验
|
药物名称 |
所属企业 |
研究状态 |
治疗方案 |
|
伏美替尼 |
艾力斯 |
临床III期(全球) |
单药 |
|
阿美替尼 |
翰森制药 |
临床III期(中国) |
单药 |
|
迈华替尼 |
华东医药 |
临床II期(中国) |
单药 |
|
苏特替尼 |
韬略生物 |
临床II期(美/中) |
单药 |
|
舒沃替尼 |
迪哲医药 |
临床II期(IIT) |
联合安罗替尼 |
|
PH001 |
浦合医药 |
临床I期(中国) |
单药 |
|
BDTX-1535 |
Black Diamond Therapeutics |
临床I/II期(美国) |
单药 |
|
ORIC-114 |
ORIC Pharmaceuticals |
临床I/II期(美国) |
单药 |
数据来源:医药魔方
此前提到,PACC突变难治的核心在于药物结合口袋空间变小导致药物无法稳定结合,因此针对该类突变亚型最直接的药物开发思路之一便为提高剂量以增加药物浓度,从而改善药物结合效率、克服疗效受限。在这个策略下,药物分子的安全性尤为重要。
以二代EGFR-TKI阿法替尼和三代EGFR-TKI伏美替尼为例,在阿法替尼的ACHILLES/TORG1834试验中提到,40mg QD(用药剂量与目前已上市的适应症相同)给药剂量会导致明显的安全性问题,三级及以上不良反应发生率高达44%2,仅23%患者可维持该剂量至治疗结束。而在伏美替尼的FURTHER试验中,给药剂量240mg QD(用药剂量为目前已上市的适应症的3倍),多数患者耐受良好,三级及以上不良反应发生率约22%3。安全性的提高进一步拉大临床给药剂量窗口,为开发针对PACC突变安全有效的药物奠定了基础。
此外,针对PACC突变的药物开发另一难点为亚型的全面覆盖。一代和二代EGFR-TKI药物的研发多早于PACC突变概念提出之前,目前临床数据仅支持在部分突变亚型中有效。随着PACC突变的概念普及,更多新一代EGFR-TKI药物在基于这类突变做大规模临床研究,纳入的亚型也越来越多样化。
在伏美替尼针对PACC突变的FURTHER试验中,除G719X、S768I突变外,还纳入了E709X、V774M等少见的突变亚型(下述统称“其他PACC亚型”)。在240mg QD给药剂量下,总体cORR约为68.2%(G719X和S768I突变亚型的总体cORR约为72.2%;其他PACC亚型的总体cORR约为50%)。未来随着纳入临床研究的患者越来越多,更多亚型的疗效数据将被揭晓。在PACC突变中,更广泛、更安全的药物一直是追求的方向。
伏美替尼FURTHER临床试验部分结果3
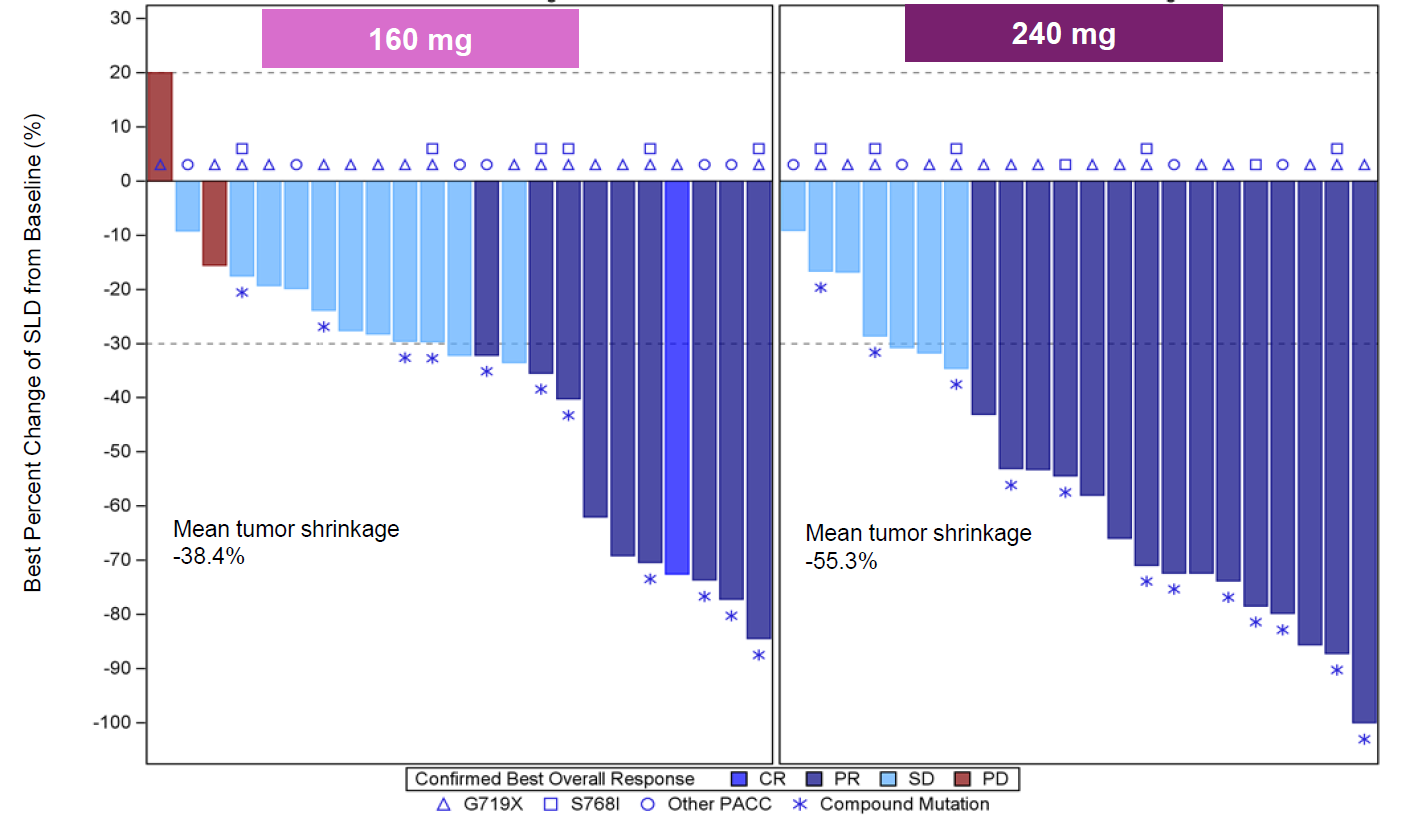
展望未来的治疗方案:精准分层、全程管理
未来,EGFR突变NSCLC患者的治疗将迈入“精准分层、疗效升级、全程管理”的新时代。随着EGFR分类体系越来越精细化,以及NGS检测技术普及度越来越高,PACC突变的精准识别率将大幅提升,为每位患者适时匹配精准的治疗方案筑牢基础。在药物研发方向,更多的EGFR-TKI药物以更大的安全窗及更高选择性的结构设计,有望实现PACC突变位点的全覆盖。
当更多针对PACC突变构象特点的新药持续涌现,临床疗效天花板将进一步提高。同时,治疗策略将更趋向个体化,基于突变亚型、共突变状态及是否合并脑转移等特征,灵活组合EGFR-TKI单药、联合治疗或高剂量方案,再配合活检动态监测耐药机制,形成“检测-治疗-随访”的闭环管理。随着专家共识与临床指南的不断完善,PACC突变患者将彻底告别疗效有限、选择匮乏的困境,迎来更高效、更安全、更具针对性的靶向治疗新图景。
参考文献:
1. JP Robichaux, et al. Structure-based classification predicts drug response in EGFR-mutant NSCLC. Nature vol. 597(2021): 732–737
2. Miura S, et al. Pragmatic randomized study of Afatinib versus chemotherapy for patients with non-small cell lung cancer with uncommon Epidermal Growth Factor Receptor mutations: ACHILLES/TORG1834. J Clin Oncol. 2025, 43(18): 2049-2058.
3. Xiuning Le, et al. Updated clinical results from FURTHER: A study of Firmonertinib in TKI-Naïve, advanced NSCLC with EGFR PACC mutations